বাস্তব গ্যাস (Real gas):
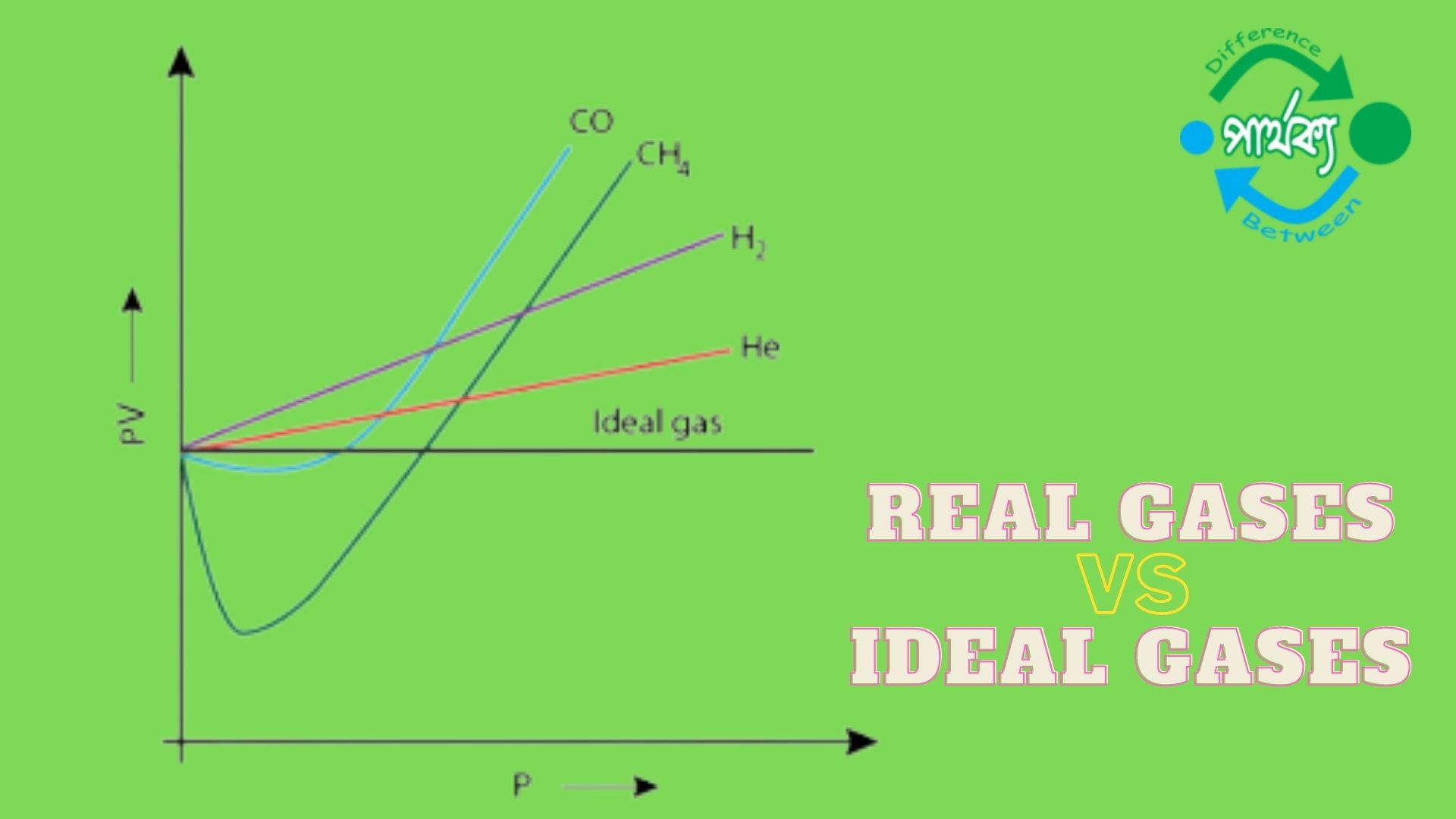
যে সব গ্যাস বয়েলের সূত্র বা চার্লসের সূত্র সঠিক ভাবে মেনে চলে না তাদের বাস্তব বা প্রকৃত গ্যাস বলে। উদাহরণ – হাইড্রোজেন, অক্সিজেন , নাইট্রোজেন প্রভৃতি গ্যাস গুলি বয়েলের সূত্র মেনে চলে না বলে এরা বাস্তব গ্যাস । আদর্শ গ্যাসের অস্তিত্ব কল্পনা মাত্র । উচ্চ উষ্ণতায় এবং নিম্নচাপে বাস্তব গ্যাসগুলি আদর্শ গ্যাসের মতো আচরন করে থাকে। PV=nRT শর্তে বাস্তব গ্যাস চার্লস ও বয়েলের সূত্র মেনে চলে |
আদর্শ গ্যাস (Ideal gas):
যে সকল গ্যাস সকল তাপমাত্রায় ও সকল চাপে গ্যাস সূত্ৰসমূহ যথা- বয়েলের সূত্র, চার্লসের সূত্র, অ্যাভােগাড্রোর সূত্র মেনে চলে তাদের আদর্শ গ্যাস বলে। আদর্শ গ্যাসের আচরণ PV = nRT সমীকরণ দ্বারা নিয়ন্ত্রিত হয়। গ্যাস আদর্শ হওয়ার জন্য একটি বিকল্প শর্ত ব্যবহার করা যায়। যেমন যে সকল গ্যাসের ক্ষেত্রে স্থির তাপমাত্রায় অভ্যন্তরীণ শক্তি আয়তনের উপর নির্ভরশীল নয় তাদেরকেও আদর্শ গ্যাস বলে।আদর্শ গ্যাস সূত্রটি পূর্বের গ্যাস সূত্রেরই অনুসিদ্ধান্ত। বাস্তব গ্যাসগুলি কম চাপ ও উচ্চ উষ্ণতায় প্রায় আদর্শ গ্যাসের মতো আচরণ করে।
কম উষ্ণতা ও চাপে বাস্তব গ্যাসগুলি আদর্শ আচরণ থেকে সম্পূর্ণ বিচ্যুত হয়, কারণ এই সময় গ্যাসগুলি অবস্থার পরিবর্তনের মাধ্যমে ঘনীভূত হয়ে তরল কিংবা অবক্ষিপ্ত হয়ে কঠিনে পরিণত হয়। বাস্তব গ্যাসের এই বিচ্যুতির পরিমাপকেই সংনম্যতা (Compressibility) বলে।
বাস্তব গ্যাস ও আদর্শ গ্যাসের মধ্যে পার্থক্যঃ
যে সব গ্যাস বয়েলের সূত্র বা চার্লসের সূত্র সঠিক ভাবে মেনে চলে না তাদের বাস্তব বা প্রকৃত গ্যাস বলে। বাস্তব গ্যাস ও আদর্শ গ্যাসের মধ্যে পার্থক্য নিম্নরূপ-
১। যে সব গ্যাস বয়েলের সূত্র বা চার্লসের সূত্র সঠিক ভাবে মেনে চলে না তাদের বাস্তব বা প্রকৃত গ্যাস বলে। অন্যদিকে, যে সকল গ্যাস সকল তাপমাত্রায় ও সকল চাপে গ্যাস সূত্ৰসমূহ যথা- বয়েলের সূত্র, চার্লসের সূত্র, অ্যাভােগাড্রোর সূত্র মেনে চলে তাদের আদর্শ গ্যাস বলে।
২। বাস্তব গ্যাস গ্যাসীয় সূত্রগুলো ও PV = nRT সমীকরণ মেনে চলে না। তবে খুব নিম্ন চাপে ও উচ্চ তাপমাত্রায় তারা গ্যাসীয় সূত্রগুলো ও PV = nRT সমীকরণ আংশিকভাবে মেনে চলে। অন্যদিকে, আদর্শ গ্যাস সকল তাপমাত্রা ও চাপে গ্যাসের সূত্রগুলো ও PV = nRT সমীকরণ মেনে চলে।
৩। প্রকৃতিতে সব গ্যাসীয় পদার্থ হল বাস্তব গ্যাস। অন্যদিকে, প্রকৃতিতে আদর্শ গ্যাসের কোনো অস্তিত্ব নেই।
৪। বাস্তব গ্যাসের ক্ষেত্রে অণুগুলোর আয়তন পাত্রের আয়তনের তুলনায় নগণ্য ধরা হয় না। অন্যদিকে, আদর্শ গ্যাসের অণুগুলোর আয়তন পাত্রের আয়তনের তুলনায় নগণ্য ধরা হয়।
৫। বাস্তব গ্যাসের ক্ষেত্রে প্রতিটি অণুর মধ্যে পারস্পরিক আকর্ষণ বল ক্রিয়া করে। অন্যদিকে, আদর্শ গ্যাসের অণুগুলোর মধ্যে কোনো আকর্ষণ বল ক্রিয়া করে না।
৬। বাস্তব গ্যাসের সংকোচনশীলতা গুণাঙ্ক Z এর মান 1 অপেক্ষা কম বা বেশি হয়। অন্যদিকে, আদর্শ গ্যাসের সংকোচনশীলতা গুণাঙ্ক Z এর মান সর্বদা 1 হয়।